5月16日,国际权威学术期刊《Cell Research》在线发表了中国科学技术大学生命科学学院蔡刚教授课题组题为“Structural basis of allosteric regulation of Tel1/ATM kinase”的研究论文,阐明了基因组稳定性调控核心激酶-ATM (ataxia-telangiectasia mutated)别构调节的分子机制。
基因组稳定性维持是一切生命活动的基础,然而,多种外源和内源因素产生的广泛 DNA损伤和复制压力,构成了基因组不稳定的主要来源。ATM和 ATR (ataxia telangiectasia and Rad3-related protein)激酶分别启动细胞对DNA双链断裂损伤和DNA单链断裂损伤/不稳定复制叉的DNA损伤应答响应。解析ATM和ATR激酶的三维结构,并在此基础上理解ATM和ATR活性严谨调控的分子机制,不仅具有阐明基因组稳定性调控的重大科学意义,也将对肿瘤放射治疗的新型增敏剂的研发起到重要指导作用。
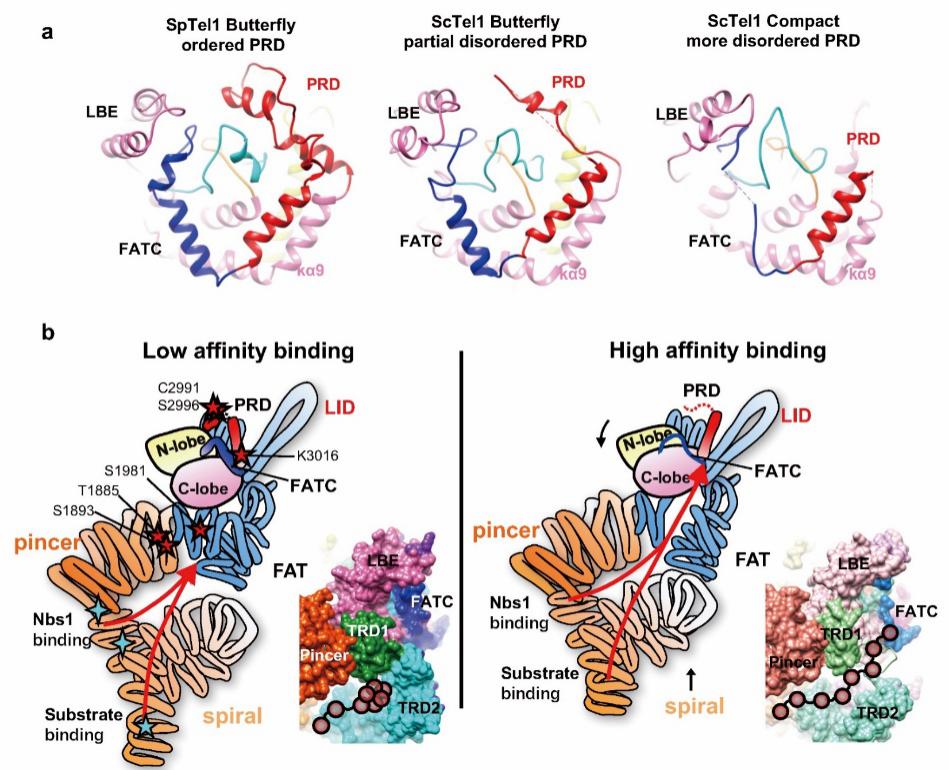
在前期工作中,蔡刚课题组报道了ATM和ATR激酶首个高分辨率冷冻电镜结构,发现并命名几个关键调控结构域、阐明其作用机理,揭示了ATM/ATR激酶活性严谨调控的分子机制(Nature Communications, 2016; Science, 2017)。然而,ATM/ATR激酶如何识别、筛选、催化底物,以及激酶活性精细调节的分子机制尚不清楚。为了回答这个重要的科学问题,蔡刚课题组解析了ATM激酶多种不同功能状态的高分辨率结构,清晰描绘了ATM激活过程的多个阶段,鉴定了ATM激酶底物募集和结合通道,并发现多种关键翻译后修饰和活化突变位点集中分布在这个通道上,揭示了ATM招募和筛选底物的机制。此外,发现ATM和ATR激酶活性中心的底物结合口袋具有高度保守的结构特征:PRD通过与活化环的直接相互作用锚定活化环、封堵底物结合口袋。ATM催化所必需的活化环的运动严格依赖PRD以及底物结合和输送通道的协同变化。本研究揭示了ATM激酶变构调节的网络,对于底物识别、招募和催化磷酸化具有重要意义。
蔡刚课题组博士研究生辛吉瑀、博士后许柱、研究员王雪娟为文章共同第一作者。该研究得到了国家自然科学基金、国家重大研究计划和和合肥微尺度物质科学国家研究中心的资助,并获得了中科院生物物理所生物成像中心的仪器和技术支持。
文章链接:https://www.nature.com/articles/s41422-019-0176-1
(生命科学学院、微尺度物质科学国家研究中心、科研部)